Газовый закон клапейрона
Оглавление:
Законы идеального газа
Конспект лекции с демонстрациями
Аннотация: традиционное изложение темы, дополненное демонстрацией на компьютерной модели.
Из трех агрегатных состояний вещества наиболее простым является газообразное состояние. В газах силы, действующие между молекулами, малы и при определенных условиях ими можно пренебречь.
Газ называется идеальным, если:
— можно пренебречь размерами молекул, т.е. можно считать молекулы материальными точками;
— можно пренебречь силами взаимодействия между молекулами (потенциальная энергия взаимодействия молекул много меньше их кинетической энергии);
— удары молекул друг с другом и со стенками сосуда можно считать абсолютно упругими.
Реальные газы близки по свойствам к идеальному при:
— условиях, близких к нормальным условиям (t = 0 0 C, p = 1.03·10 5 Па);
— при высоких температурах.
Законы, которым подчиняется поведение идеальных газов, были открыты опытным путем достаточно давно. Так, закон Бойля — Мариотта установлен еще в 17 веке. Дадим формулировки этих законов.
Закон Бойля — Мариотта. Пусть газ находится в условиях, когда его температура поддерживается постоянной (такие условия называются изотермическими).Тогда для данной массы газа произведение давления на объем есть величина постоянная:

Эту формулу называют уравнением изотермы. Графически зависимость p от V для различных температур изображена на рисунке.

Свойство тела изменять давление при изменении объема называется сжимаемостью. Если изменение объема происходит при T=const, то сжимаемость характеризуется изотермическим коэффициентом сжимаемости  который определяется как относительное изменение объема, вызывающее изменение давления на единицу.
который определяется как относительное изменение объема, вызывающее изменение давления на единицу.

Для идеального газа легко вычислить его значение. Из уравнения изотермы получаем:


Знак минус указывает на то, что при увеличении объема давление уменьшается. Т.о., изотермический коэффициент сжимаемости идеального газа равен обратной величине его давления. С ростом давления он уменьшается, т.к. чем больше давление, тем меньше у газа возможностей для дальнейшего сжатия.
Закон Гей — Люссака. Пусть газ находится в условиях, когда постоянным поддерживается его давление (такие условия называются изобарическими). Их можно осуществить, если поместить газ в цилиндр, закрытый подвижным поршнем. Тогда изменение температуры газа приведет к перемещению поршня и изменению объема. Давление же газа останется постоянным. При этом для данной массы газа его объем будет пропорционален температуре:

где V0 — объем при температуре t = 0 0 C,  — коэффициент объемного расширения газов. Его можно представить в виде, аналогичном коэффициенту сжимаемости:
— коэффициент объемного расширения газов. Его можно представить в виде, аналогичном коэффициенту сжимаемости:

Графически зависимость V от T для различных давлений изображена на рисунке.

Перейдя от температуры в шкале Цельсия к абсолютной температуре  , закон Гей — Люссака можно записать в виде:
, закон Гей — Люссака можно записать в виде:

Закон Шарля. Если газ находится в условиях, когда постоянным остается его объем (изохорические условия), то для данной массы газа давление будет пропорционально температуре:

где р0 — давление при температуре t = 0 0 C,  — коэффициент давления. Он показывает относительное увеличение давления газа при нагревании его на 1 0 :
— коэффициент давления. Он показывает относительное увеличение давления газа при нагревании его на 1 0 :

Закон Шарля также можно записать в виде:

Закон Авогадро: один моль любого идеального газа при одинаковых температуре и давлении занимает одинаковый объем. При нормальных условиях (t = 0 0 C, p = 1.03·10 5 Па) этот объем равен  м -3 /моль.
м -3 /моль.
Число частиц, содержащихся в 1 моле различных веществ, наз. постоянная Авогадро:

Легко вычислить и число n0 частиц в 1 м 3 при нормальных условиях:

Это число называется числом Лошмидта.
Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов, т.е.

где  — парциальные давления — давления, которые бы оказывали компоненты смеси, если бы каждый из них занимал объем, равный объему смеси при той же температуре.
— парциальные давления — давления, которые бы оказывали компоненты смеси, если бы каждый из них занимал объем, равный объему смеси при той же температуре.
Уравнение Клапейрона — Менделеева. Из законов идеального газа можно получить уравнение состояния, связывающее Т, р и V идеального газа в состоянии равновесия. Это уравнение впервые было получено французским физиком и инженером Б. Клапейроном и российским учеными Д.И. Менделеевым, поэтому носит их имя.
Пусть некоторая масса газа занимает объем V1, имеет давление p1 и находится при температуре Т1. Эта же масса газа в другом состоянии характеризуется параметрами V2, p2, Т2 (см. рисунок). Переход из состояния 1 в состояние 2 осуществляется в виде двух процессов: изотермического (1 — 1′) и изохорического (1′ — 2).

Для данных процессов можно записать законы Бойля — Мариотта и Гей — Люссака:


Исключив из уравнений p1 ‘ , получим

Так как состояния 1 и 2 были выбраны произвольно, то последнее уравнение можно записать в виде:

Это уравнение называется уравнением Клапейрона, в котором В — постоянная, различная для различных масс газов.
Менделеев объединил уравнение Клапейрона с законом Авогадро. Согласно закону Авогадро, 1 моль любого идеального газа при одинаковых p и T занимает один и тот же объем Vm, поэтому постоянная В будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называется универсальной газовой постоянной. Тогда

Это уравнение и является уравнением состояния идеального газа, которое также носит название уравнение Клапейрона — Менделеева.
Числовое значение универсальной газовой постоянной можно определить, подставив в уравнение Клапейрона — Менделеева значения p, T и Vm при нормальных условиях:

Уравнение Клапейрона — Менделеева можно записать для любой массы газа. Для этого вспомним, что объем газа массы m связан с объемом одного моля формулой V=(m/M)Vm, где М — молярная масса газа. Тогда уравнение Клапейрона — Менделеева для газа массой m будет иметь вид:

где  — число молей.
— число молей.
Часто уравнение состояния идеального газа записывают через постоянную Больцмана:

Исходя из этого, уравнение состояния можно представить как

где  — концентрация молекул. Из последнего уравнения видно, что давление идеального газа прямо пропорционально его температуре и концентрации молекул.
— концентрация молекул. Из последнего уравнения видно, что давление идеального газа прямо пропорционально его температуре и концентрации молекул.
Небольшая демонстрация законов идеального газа. После нажатие кнопки «Начнем» Вы увидите комментарии ведущего к происходящему на экране (черный цвет) и описание действий компьютера после нажатия Вами кнопки «Далее» (коричневый цвет). Когда компьютер «занят» (т.е. идет опыт) эта кнопка не активна. Переходите к следующему кадру, лишь осмыслив результат, полученный в текущем опыте. (Если Ваше восприятие не совпадает с комментариями ведущего, напишите!)
Вы можете убедиться в справедливости законов идеального газа на имеющейся компьютерной модели самостоятельными измерениями.
teachmen.ru
Объединение учителей Санкт-Петербурга
Основные ссылки
Уравнение состояния идеального газа. Газовые законы.
Уравнение состояния идеального газа
(уравнение Менделеева – Клапейрона).
Уравнением состояния называется уравнение, связывающее параметры физической системы и однозначно определяющее ее состояние.
В 1834 г. французский физик Б. Клапейрон, работавший дли тельное время в Петербурге, вывел уравнение состояния идеального газа для постоянной массы газа. В 1874 г. Д. И. Менделеев вывел уравнение для произвольного числа молекул.
В МКТ и термодинамике идеального газа макроскопическими параметрами являются: p, V, T, m.
Мы знаем, что 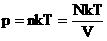 . Следовательно,
. Следовательно, 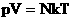 . Учитывая, что
. Учитывая, что 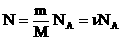 , получим:
, получим: 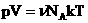 .
.
Произведение постоянных величин есть величина постоянная, следовательно: 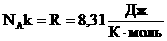 — универсальная газовая постоянная (универсальная, т.к. для всех газов одинаковая).
— универсальная газовая постоянная (универсальная, т.к. для всех газов одинаковая).
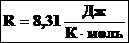
Таким образом, имеем:
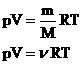 — уравнение состояния (уравнение Менделеева – Клапейрона).
— уравнение состояния (уравнение Менделеева – Клапейрона).

Другие формы записи уравнения состояния идеального газа.
1.Уравнение для 1 моля вещества.
Если n=1 моль, то, обозначив объем одного моля Vм, получим: 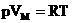 .
.
Для нормальных условий получим: 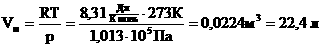

2. Запись уравнения через плотность: 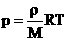 — плотность зависит от температуры и давления!
— плотность зависит от температуры и давления!
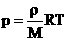
3. Уравнение Клапейрона.
Часто необходимо исследовать ситуацию, когда меняется состояние газа при его неизменном количестве (m=const) и в отсутствие химических реакций (M=const). Это означает, что количество вещества n=const. Тогда: 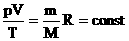
Эта запись означает, что для данной массы данного газа справедливо равенство: 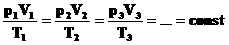
Для постоянной массы идеального газа отношение произведения давления на объем к абсолютной температуре в данном состоянии есть величина постоянная: 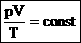 .
.

Газовые законы.
1. Закон Авогадро.
В равных объемах различных газов при одинаковых внешних условиях находится одинаковое число молекул (атомов).
Доказательство: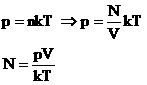
Следовательно, при одинаковых условиях (давление, объем, температура) число молекул не зависит от природы газа и одинаково.
2. Закон Дальтона.
Давление смеси газов равно сумме парциальных (частных) давлений каждого газа.
Доказательство: 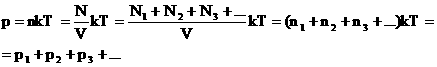
3. Закон Паскаля.
Давление, производимое на жидкость или газ, передается во все стороны без изменения.
www.eduspb.com
Закон Менделеева-Клапейрона

Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Клапейрона — Менделеева) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
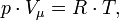
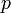 — давление,
— давление,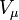 — молярный объём,
— молярный объём,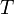 — абсолютная температура,
— абсолютная температура,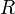 — универсальная газовая постоянная.
— универсальная газовая постоянная.
Так как 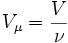 , где
, где 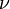 — количество вещества, а
— количество вещества, а 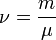 , где
, где 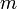 — масса,
— масса, 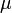 — молярная масса, уравнение состояния можно записать:
— молярная масса, уравнение состояния можно записать:
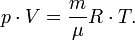
Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
В случае постоянной массы газа уравнение можно записать в виде:
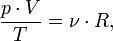
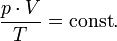
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
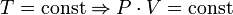 — закон Бойля — Мариотта.
— закон Бойля — Мариотта. 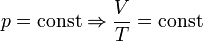 — закон Гей-Люссака.
— закон Гей-Люссака. 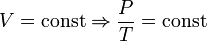 — закон Шарля (второй закон Гей-Люссака, 1808 г.)
— закон Шарля (второй закон Гей-Люссака, 1808 г.)
С точки зрения химика этот закон может звучать несколько иначе: Объёмы вступающих в реакцию газов при одинаковых условиях (температуре, давлении) относятся друг к другу и к объёмам образующихся газообразных соединений как простые целые числа. Например, 1 объём водорода соединяется с 1 объёмом хлора, при этом образуются 2 объёма хлороводорода:
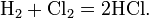
1 объём азота соединяется с 3 объёмами водорода с образованием 2 объёмов аммиака:
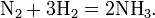
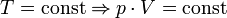 — закон Бойля — Мариотта.
— закон Бойля — Мариотта.
Закон Бойля — Мариотта назван в честь ирландского физика, химика и философа Роберта Бойля (1627—1691), открывшего его в 1662 г., а также в честь французского физика Эдма Мариотта (1620—1684), который открыл этот закон независимо от Бойля в 1676 году.
В некоторых случаях (в газовой динамике) уравнение состояния идеального газа удобно записывать в форме
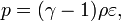
где 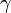 — показатель адиабаты,
— показатель адиабаты,  — внутренняя энергия единицы массы вещества.
— внутренняя энергия единицы массы вещества.
Эмиль Амага обнаружил, что при высоких давлениях поведение газов отклоняется от закона Бойля — Мариотта. И это обстоятельство может быть прояснено, как считал ещё М. В. Ломоносов, на основании молекулярных представлений.
С одной стороны, в сильно сжатых газах размеры самих молекул являются сравнимыми с расстояниями между молекулами. Таким образом, свободное пространство, в котором движутся молекулы, меньше, чем полный объем газа. Это обстоятельство увеличивает число ударов молекул в стенку, так как благодаря ему сокращается расстояние, которое должна пролететь молекула, чтобы достигнуть стенки.
С другой стороны, в сильно сжатом и, следовательно, более плотном газе молекулы заметно притягиваются к другим молекулам гораздо большую часть времени, чем молекулы в разреженном газе. Это, наоборот, уменьшает число ударов молекул в стенку, так как при наличии притяжения к другим молекулам молекулы газа движутся по направлению к стенке с меньшей скоростью, чем при отсутствии притяжения. При не слишком больших давлениях. более существенным является второе обстоятельство и произведение 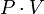 немного уменьшается. При очень высоких давлениях большую роль играет первое обстоятельство и произведение
немного уменьшается. При очень высоких давлениях большую роль играет первое обстоятельство и произведение 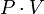 увеличивается.
увеличивается.
Связь с современной физикой
В [1] и [2] показано, что уравнение состояния идеального газа может быть получено из соотношения неопределенностей Гейзенберга. Точнее, «…уравнение газового состояния … есть не что иное, как одна из форм записи соотношения неопределенностей Гейзенберга» [1] .
dic.academic.ru
главная > справочник > химическая энциклопедия:
Клапейрона-Менделеева уравнение, уравнение состояния идеального газа, устанавливающее связь между его объемом V. давлением р и абс. температурой Т. Имеет вид:
где n — число молей газа, R = 8,31431 Дж/моль.К) — газовая постоянная. Для 1 моля газа pv=RT, где v-молярный объем. Клапейрона-Менделеева уравнение записывают также в форме: pV=NkT, где N — число частиц газа в объеме V, k — постоянная Больцмана.
Если М — масса газа, а m — его мол. масса, то pV=(M/m)RT. К.-М. у. приближенно выполняется для реальных газов при достаточно низких давлениях; с повышением температуры область давлений, при которых состояние реального газа можно описывать Клапейрона-Менделеева уравнением, расширяется. Для молекулярных газов (напр., атм. воздуха) при обычных температурах и давлениях до 1,01 . 10 5 Па (1 атм) Клапейрона-Менделеева уравнение выполняется достаточно точно. Клапейрона-Менделеева уравнение широко используют при расчетах термодинамич. свойств газов, определения работы, совершаемой системой в к.-л. процессе. Ассоциированные газы, например пары НСООН, СН3СООН, С3Н7СООН и др. карбоновых кислот, не подчиняются Клапейрона-Менделеева уравнению даже при очень низких давлениях.
Уравнение было установлено опытным путем Б. П. Э. Клапейроном в 1834; оно имело вид: pV=ВТ, где В — постоянная, зависящая от природы газа и его массы. В совр. виде уравнение было получено в 1874 для 1 моля идеального газа Д. И. Менделеевым в результате объединения законов Гей — Люссака, Бойля-Мариотта и Авогадро. Вывод Клапейрона-Менделеева уравнения возможен на основании представлений молекулярно-кинетич. nеории газов (cv. Газы). ©Н. А. Смирнова,
выберите первую букву в названии статьи: А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
www.chemport.ru
Объединенный газовый закон (уравнение Клапейрона)
Газовые законы
Всего есть три (основных) газовых закона и, соответственно, три процесса:
-закон Шарля — изохорный процесс (m,V-const) (линия на графике — изохора)
-закон Гей-Люссака — изобарный процесс (m,p-const) (линия на графике — изобара)
-закон Бойля-Мариотта — изотермический процесс (m,T-const) (линия на графике — изотерма)
Есть еще адиабатный процесс (линия на графике — адиабата), объединенный газовый закон — уравнение Клапейрона и уравнение состояния идеального газа — уравнение Менделеева-Клапейрона.
Они все описывают состояние газа. Состояние газа характеризуется объемом, давлением, температурой и массой. Сразу скажу, что масса во всех трех газовых законах не изменяется (m=const), а для остальных величин есть как раз эти самые законы.
Вообще, в газовых законах (да и не только в них) должна использоваться термодинамическая (она же абсолютная) температура, то есть единицы измерения — Кельвины. Но мало ли какое может быть условие. Поэтому, для удобства, в рассчетной форме ниже можно выбирать единицы измерения температуры (Кельвины и градусы Цельсия).
Также для конвертирования температур (и других величин) можете воспользоваться конвертером.
Объединенный газовый закон
Вроде понятно, что p1V1/T1=p2V2/T2 , но как это получили? А вот как:
Давление идеального газа равно: p=nkT.
n — концентрация, равная: n=N/V. Тогда: p=NkT/V
Если масса газа постоянна (m=const) и число частиц, получается тоже (N=const), то уравнение давления можно записать как:
pV/T=Nk=const
Вот и получили, что произведение давления на объем, и все это поделенное на температуру — имеет постоянное значение.
Из объединенного газового закона получаются все остальные газовые законы (закон Шарля, закон Гей-Люссака, закон Бойля-Мариотта)
fizlite.ru
